重点实验室在抗前列腺癌药物研究中获取进展
近日,中国科学院再生生物学重点实验室、广东省干细胞与再生医学重点实验室吴东海团队,中国科学院广州生物医药与健康研究院许永团队与澳大利亚联邦科学与工业研究组织Craig L. Francis团队共同在European Journal of Medicinal Chemistry期刊上发表了题为“1-Benzyloxy-5-phenyltetrazole derivatives highly active against androgen receptor-dependent prostate cancer cells”的研究论文。研究发现一类1-苄氧基-5-苯基四氮唑衍生物可以有效降低雄激素受体及其变异体AR-V7的表达,抑制去势抵抗性前列腺癌细胞和异种移植的去势抵抗性前列腺癌小鼠肿瘤的生长。
前列腺癌是严重威胁全球男性健康的第二大癌症。前列腺癌患者在治疗过程中会出现耐药现象,形成去势抵抗性前列腺癌,这为临床的治疗增加了难度。前列腺癌细胞的存活和生长依赖雄激素-雄激素受体信号(androgen-androgen receptor,AR)的持续激活。在去势抵抗性前列腺中更是出现了雄激素受体突变、雄激素受体剪切变异体(AR-V7)激活、雄激素受体转录增多和雄激素受体共调节因子表达增加等问题,这也是前列腺癌产生耐药的原因。迄今为止,靶向雄激素-雄激素受体信号通路是去势抵抗性前列腺癌最主要的治疗方式。因此,基于雄激素-雄激素受体信号通路进行药物开发具有重要临床意义。
在本课题中,研究人员利用前列腺癌细胞系22Rv1(雄激素依赖性生长,高表达AR和AR-V7)和PC3(雄激素非依赖性生长)筛选了澳大利亚CSIRO 的25000个小分子化合物,并获得了具有1-苄氧基-5-苯基四氮唑类母核结构的苗头化合物。结构改造和优化后,研究人员对一系列1-苄氧基-5-苯基四氮唑衍生物和类似物进行了生物活性评估。结果表明,活性最好的化合物在22Rv1细胞上的IC50<50nM。先导化合物既可以下调雄激素受体和其变异体AR-V7的蛋白表达,又能调控雄激素受体信号通路相关基因的表达。先导化合物可以有效抑制22Rv1异种移植的去势抵抗性前列腺癌小鼠肿瘤生长,抑瘤率约为53%。该研究为临床治疗前列腺癌药物的开发提供了潜在的候选化合物。相关研究成果在2022年2月25日申请1项专利(202210177099.7)。
重点实验室吴东海课题组博士后赵世亭为论文第一作者;澳大利亚联邦科学与工业研究组织Craig L. Francis教授、中国科学院广州生物医药与健康研究院许永研究员、吴东海研究员为共同通讯作者。该研究得到了CSIRO-CAS国际合作项目、广州国际合作项目、中国国家重点研发计划和中国科学院重点国际合作项目等的资助。
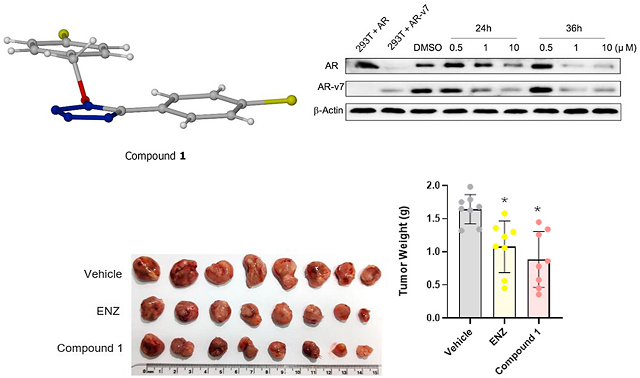
图注:先导化合物Compound 1的结构(左上);先导化合物Compound 1抑制22Rv1细胞AR和AR-V7的蛋白表达(右上);先导化合物Compound 1抑制22Rv1异种移植的去势抵抗性前列腺癌小鼠肿瘤生长(下)