重点实验室揭示CCR8可作为治疗T细胞恶性肿瘤潜在的治疗靶点
成人T淋巴细胞白血病/淋巴瘤(ATLL)是由HTLV-1感染成熟CD4 T细胞所引起的T细胞恶性肿瘤。ATLL和外周血T细胞淋巴瘤是两种发病率最高的淋巴瘤。虽然化疗能够提高ATLL患者的治疗效果,但是化疗无法延长ATLL患者的生存期。此外,ATLL患者的5年生存率仍然不容乐观。因此,亟需寻找用于治疗ATLL患者更有效的治疗方法。CAR T细胞在治疗急性B淋巴细胞白血病方面已取得突破性进展,但CAR T细胞在治疗T细胞恶性肿瘤方面仍然存在许多挑战,可能的原因包括缺乏特异性的肿瘤抗原、T细胞扩增受限、异体回输以及基因编辑技术不成熟等。因此,寻找特异性的肿瘤抗原,从而提高CAR T细胞治疗T细胞恶性肿瘤的治疗效果意义重大。
5月26号,中国科学院再生生物学重点实验室、广东省干细胞与再生医学重点实验室李鹏研究员课题组在Frontiers in immunology上发表了题为The Chemokine Receptor CCR8 Is a Target of Chimeric Antigen T Cells for Treating T Cell Malignancies的研究,为临床上CCR8阳性的T细胞恶性肿瘤患者提供新的治疗策略。
ATLL细胞会表达与调节性T细胞(Treg细胞)相关且具有一定的免疫抑制的作用的靶标,如CD4、CD25、FXOP3和CCR4等,猜测可能起源于Treg细胞。针对Treg细胞疗法,目前对CCR8单抗的研究最为热门。CCR8单抗能够特异性清除肿瘤组织的Treg细胞,并不会影响外周血的Treg细胞。这表明CCR8具有很好的特异性和安全性。
首先,研究团队在临床肿瘤样本和肿瘤细胞系上证明了ATLL表达高水平的CCR8。接着,研究团队构建了2种靶向CCR8 CAR T细胞,并发现靶向CCR8 CAR T细胞不会攻击自身细胞,从而不会产生严重的自残现象,因此不影响自身CAR T细胞的扩增。在人源化小鼠模型中验证了靶向CCR8 CAR T细胞对CCR8阳性的ATLL细胞具有良好的杀伤活性,而靶向CD7 CAR T细胞对急性T淋巴细胞白血病(T-ALL)患者虽然具有一定的疗效,但患者常常会发生肿瘤复发。此外,研究团队还发现Jurkat细胞(T-ALL细胞的一种)也表达CCR8,且靶向CCR8 CAR T细胞有效抑制了Jurkat细胞的肿瘤进展。本研究为表达CCR8阳性的肿瘤患者(不仅是血液肿瘤也包含实体肿瘤)提供了一种新的治疗方法和治疗策略。
该研究工作主要由广州健康院重点实验室郑迪威博士和生物岛实验室王新东共同完成,广州健康院重点实验室李鹏研究员为本文通讯作者。该研究成果得到了国家重点研发计划-战略性科技创新合作项目、国家自然科学基金面上项目、广东省新药创制项目和国自然国际合作研究项目的支持。
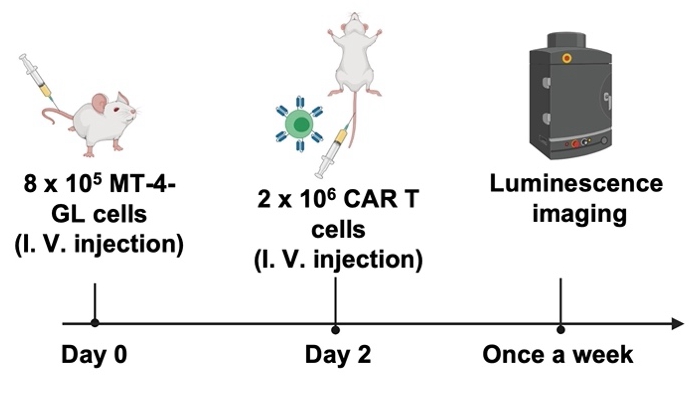
靶向CCR8 CAR T细胞治疗MT-4小鼠模型的流程图