重点实验室在肿瘤免疫治疗小鼠模型构建上获进展
10月2日,中国科学院再生生物学重点实验室李鹏课题组在国际期刊mAbs上在线发表了新的动物模型研究成果“Establishment of peripheral blood mononuclear cell-derived humanized lung cancer mouse models for studying efficacy of PD-L1/PD-1 targeted immunotherapy”。该研究探索了利用患者外周血淋巴细胞快速建立小鼠模型的方法,并首次建立了免疫系统与肿瘤组织来源于同一患者的小鼠模型。
近年来,随着免疫检查点机制的阐明与嵌合抗原受体T细胞技术的发展,免疫疗法成为治疗肿瘤的最新方向。小鼠模型是研究与评估肿瘤免疫治疗的常用模型,其中,在小鼠体内重建人免疫系统是建立动物模型的关键。然而,目前广泛应用的小鼠模型并没有统一的重建人类免疫系统的方法与标准,对肿瘤免疫疗法的临床前研究与疗效评估造成一定的阻碍。在该研究中,研究人员首先利用不同来源的免疫细胞在免疫缺陷的小鼠体内成功重建了免疫系统,再进一步地建立携带肺癌患者肿瘤的异种移植模型,利用靶向PD-1/PD-L1的抗体进行治疗用以评估免疫重建的效率与治疗效果。该研究首次对比了不同方法在重建免疫系统效率上的差异,探索了利用患者外周血淋巴细胞快速建立小鼠模型的方法。
目前广泛应用的小鼠模型是采用健康供者的细胞重建免疫系统的,对肿瘤组织产生异体间的免疫排斥,不能精准地反应免疫疗法对肿瘤的治疗效果。该研究首次从肺癌患者的肿瘤组织中分离浸润性T细胞,与肿瘤共同移植,建立了“升级版”的小鼠模型:在同一小鼠体内携带同一患者的免疫细胞与肿瘤组织。
该研究系统对比了建立肿瘤免疫治疗的小鼠模型的方法,探索了利用外周血淋巴细胞快速建立小鼠模型的优势;同时建立了免疫系统与肿瘤组织来源于同一患者的小鼠模型,新的模型能更真实地模拟患者的体内环境,为肿瘤免疫治疗提供了更精准的研究与评价工具。
该研究获得中科院战略先导项目,广东省和广州市的经费支持。
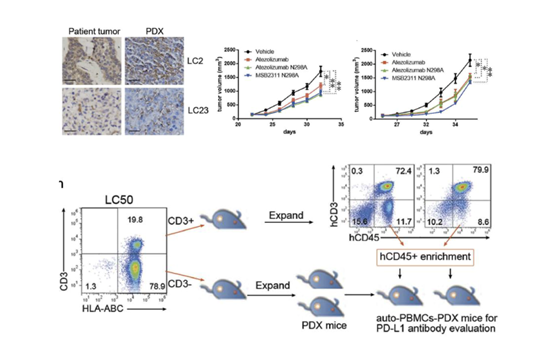
利用病人肺癌与免疫共存PDX模型临床前评估PD-1单克隆抗体疗效