重点实验室等合作揭示新冠病毒感染导致急性呼吸窘迫症的细胞机理
时间:2020-07-29
来源:广州健康院
时间:2020-07-29 来源:广州健康院
7月16日,中科院再生生物学重点实验室与生物岛实验室、广州市第八人民医院合作在Protein & Cell杂志以“Single-cell analysis reveals bronchoalveolar epithelial dysfunction in COVID-19 patients” 为题发表了新冠病人急性呼吸窘迫症致病机理方面的研究。
肺是新冠病毒感染的主要器官,目前大部分新冠病人的直接死因源于呼吸衰竭导致的急性呼吸窘迫症(ARDS)。ARDS是新冠危重症患者的主要病症,同时病程极长,导致重症监护室(ICU)资源急剧耗尽,因此,新冠危重症的ARDS病理机制研究对于有效应对疫情具有重要意义。临床检测及尸检结果表明,重症新冠病人病毒感染后会刺激肺产生大量凝胶状流动性极差的粘液,这些粘液会堵塞支气管甚至肺泡,使正常呼吸气体交换受阻,是造成重症患者ARDS的重要原因之一。目前,新冠病人粘液从何而来并不清楚,因此,了解新冠病人粘液产生的来源及原因对临床治疗具有重要指导意义。
基于上述关键问题,研究团队通过收集新冠病人肺泡灌洗液进行单细胞转录组测序(scRNA-seq),发现黏蛋白家族相关基因MUC5AC和MUC5B等在在病人中显著高表达,同时主要来源于一种称为Club的上皮细胞,说明新冠病人粘液主要来源于肺Club细胞。研究同时发现病毒感染后,纤毛生成及细结构相关基因如FOXJ1, RFX3,IFT27,DNAI2等表达显著下降,同时,ATP合酶基因表达显著升高,表明ATP含量会升高,之前的研究表明,ATP刺激能够导致粘液分泌上调数千倍。上述结果表明病毒感染后导致Club细胞粘液过度分泌,同时纤毛活性下降,这就导致了本来分泌过多的粘液更加无法正常排出体外。进一步会导致这些粘液在肺部过度堆积,直至最后堵塞了肺内部的支气管,导致呼吸衰竭。机理上,研究团队发现,病毒感染后,肺泡巨噬细胞会分泌细胞因子CCL2招募单核/中心粒细胞到受感染的区域从而被激活,这些被激活的单核/中心粒细胞会进一步分泌促炎因子IL-1β以及其他细胞因子如CXCL8、CCL3/4等, IL-1β会进一步刺激Club细胞导致粘液过度分泌,指示IL-1β可能是新冠治疗比较合适的药物靶点之一。值得一提的是,在本研究审稿期间,发表于国际医学期刊Lancet Rheumatol上的一项回顾性研究发现,针对COVID-19病人使用IL-1β拮抗剂治疗,72%的病人的病情得到了明显好转。
重点实验室、生物岛实验室陈捷凯研究员,广州市第八人民医院重症医学科邓西龙主任,中国科学院广州生物医药与健康研究院陈新文研究员为本研究的共同通讯作者。本研究得到广州医科大学呼吸疾病国家重点实验室赵金存研究员的大力合作和钟南山院士的指导。
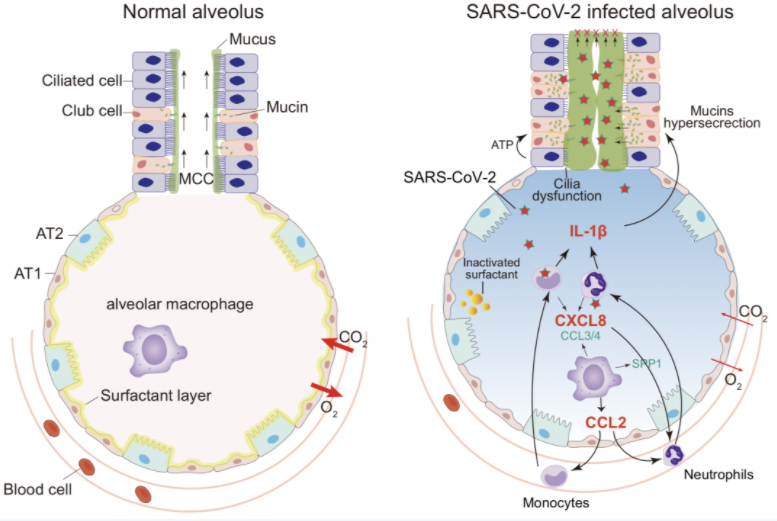
新冠病毒感染导致粘液过度分泌及纤毛受损分子机理示意图