近日,中国科学院再生生物学重点实验室Igor Samokhvalov研究员团队在Haematologica (血液)杂志发表了题为“MYB bi-allelic targeting abrogates primitive clonogenic progenitors while the emergence of primitive blood cells is not affected”的文章。本文作者Shah等人利用TALEN介导的基因编辑技术在人胚胎干细胞中对MYB基因进行了双等位基因敲除并插入了一个荧光报告基因。他们采用一种效率高、分化谱系全、重复性好的独创分化方案,对野生型和突变型人胚胎干细胞系的造血发育进行了比较研究。该分化体系培养条件明确,且不添加任何造血细胞因子,很好地模拟了人类胚胎的早期造血发育过程。
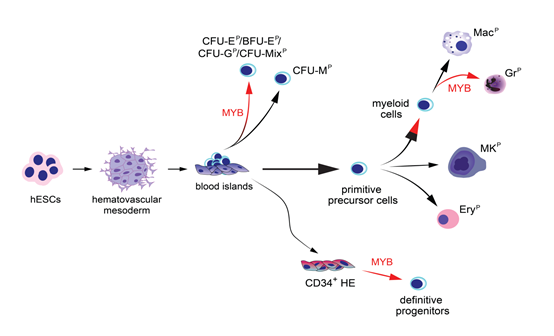
该研究结果表明,MYB对原始造血祖细胞的发育是必不可少的,但在缺乏MYB的情况下,早期人类血细胞的生成并没有受到影响。这一结果也明确表明,人类早期血细胞的生成并不依赖于造血祖细胞的出现。该研究发现在经历一个类似被称之为内皮细胞向造血细胞转变(endothelial-to-hematopoietic transition,EHT)的过程中,大量血细胞直接从造血内皮细胞中产生。该研究揭示了一个完整的来源于EHT的早期血细胞发育阶段,该过程不依赖于具有集落形成能力的造血祖细胞参与。因此,早期人类血细胞和原始造血祖细胞的发育表现为两个独立的细胞谱系(见下图)。
这项研究的另一个重要意义是阐明了MYB在人类原始造血中的作用,先前MYB被广泛认为是只在永久造血过程中起作用的转录因子。因此Shah等人的研究结果对人类血液发育领域具有非常重要的意义,因为它揭示了其他模式动物作为人类血液学研究模型的局限性。这项研究突破了血液发育领域至少两个长期存在的教条,这也可能是这一重要发现未能在国际顶级期刊上发表的原因。尽管如此,这篇文章也印证了一条作为科学家的准则:“你在哪里发表并不重要,重要的是你发表了什么”。
本研究获科技部国家重点研发计划、重大科学研究项目(973)、中国科学院再生生物学重点实验室和广东省干细胞与再生医学重点实验室的经费支持。
MYB基因在人胚胎干细胞的造血分化中的作用